物理的・化学的性質
- 外観
- 気体:無色・無臭、水分と作用して弱い酸味と刺激臭を感じます。
- 液体:無色・透明
- 個体:半透明・乳白色
- 化学名二酸化炭素
- 化学式CO2
- 分子量44.01
- 密度
- 気体:1.977kg/m3(0℃、0.1013MPa)
- 液体:1.030kg/L(−20℃、1.967MPa)
- 個体:1.566kg/L(−80℃)
- 三重点−56.6℃、0.518MPa
- 臨界温度31.1℃
- 臨界圧力7.382MPa
- PH値3.7(25℃、0.1013MPa飽和 水)
一般的性質と注意点
- 不燃性ガス
炭酸ガスは不燃性で燃焼を助けないため、消火用ガスに使用されています。 - 空気より重い
気体の炭酸ガスは空気の約1.5倍の重さがあり、換気の不十分な場所では、床の方から濃度の高い層としてたまっていきま す。炭酸ガスの使用時には換気にご注意ください。 - 水に溶けやすい
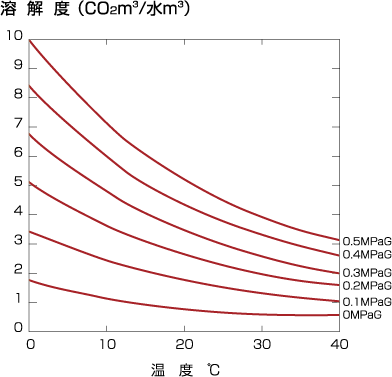
15℃の水1m3に対して約1m3の炭酸ガスが溶けます。温度が低いほど、また圧力が高いほど溶解度は大きくなります。 - 静電気の発生
液化炭酸ガスの噴出時には多量の静電気が発生します。可燃性混合気体や可燃物への着火、引火をもたらす場合がありますので、十分ご注意ください。 - 低温
固体の炭酸ガス(ドライアイス)は約−80℃と大変冷たく、また液化炭酸ガスも−20℃の低温で供給されているものもあります。取り扱いの際は凍傷にご注意ください。 - 高圧ガス
液化炭酸ガスは高圧ガス保安法の対象になります。使用・取り扱いに際しては法令の遵守が条件となります。また気体の炭 酸ガスで圧力が1MPa以上の場合も同様です。 - 人体への影響
炭酸ガスは濃度が高いと人体に悪影響を及ぼします。労働安全衛生規則では炭酸ガス濃度1.5% 以上、および酸素濃度18%未満の場所へ立ち入りを禁止しています。また日本産業衛生学会ではじょ限界として0.5% を勧告しています。なお酸 素濃度18% の場合でも炭酸ガス濃度が13.9%となる場合がありますので、必ず炭酸ガス濃度を測定する必要があります。
| 濃度(%) | 影響(通常の酸素濃度における) |
|---|---|
| 0.035 | 正常空気 |
| 0.5 | じよ限界(長期安全限界) |
| 1.5 | 立ち入り禁止。(基礎的生理機能に影響を及ぼさずに長時間にわたって耐えることはできるが、カルシウム・リン代謝に影響の出る場合がある) |
| 2.0 | 呼吸が深くなる:一回の呼吸量が30%増加 |
| 3.0 | 作業性低下:生理機能の変化が体重、血圧、心拍数などの変化として現れる。 |
| 4.0 | 呼吸がさらに深くなる:呼吸数増加、軽度のあえぎ状態:相当な不快感。 |
| 5.0 | 呼吸が極度に困難になる:重度のあえぎ:多くの人がほとんど耐えられない状態になる:悪心(吐気)の出現する場合がある:30 分の暴露で中毒症状。 |
| 7〜9 | 許容限界:激しいあえぎ:約15 分で意識不明。 |
| 10〜11 | 調整機能不能:約10分で意識不明。 |
| 15〜20 | さらに重い症候を示す。 |
| 25〜30 | 呼吸低下:血圧降下:昏睡:反射能力喪失:麻痺:数時間後に死に至る。 |
- 味覚への影響
炭酸ガスが水に溶けると、弱い酸味や弱い刺激性の臭気を感じる場合があります。水や水分の多い食品に使用する場合は注意が必要です。 - 腐食性
乾燥状態では腐食性はありませんが、水分に溶け込むと弱酸性となり、金属を腐食します。 炭酸ガスで圧力が1MPa以上の場合も同様です。
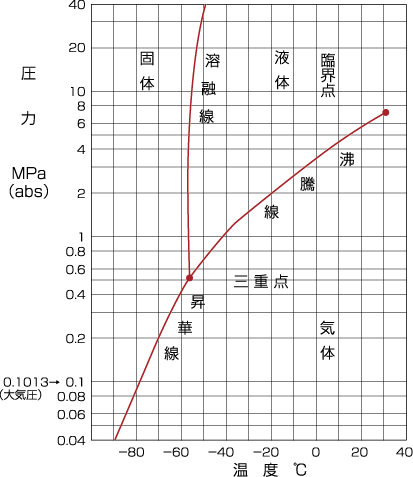
炭酸ガスの状態図
- ①沸騰線は液体と気体の相変化、昇華線は固体と気体の相変 化、溶融線は固体と液体の相変化を表します。
- ②気体の炭酸ガスを圧縮・冷却すると液体になります。
- ③臨界温度(31.1℃)を越えると圧縮しても液化しません。 なお臨界温度で液化を始める圧力(7.382MPa)を臨界圧力といいます。
- ④液体の炭酸ガスを冷却していくと、−56.6℃、0.518MPaで固体になります。この時、固体・液体・気体の状態が同時に存在するので、この点を三重点といいます。
- ⑤三重点未満の圧力では液体の状態は存在しません。したがって、大気圧では液体は存在せず、固体(ドライアイス)は直接気体に変わります。
- ⑥通常貯槽や容器に充填されている液体の炭酸ガスは、沸騰 線上の状態にあります。したがってこれらを減圧すると、液体は沸騰を始めるとともに、温度が下がって行き、三重点を下回ると内部の液体は気体と固体に変化してしまいます。
出典:液化炭酸ガス取扱テキスト 平成18年5月改定
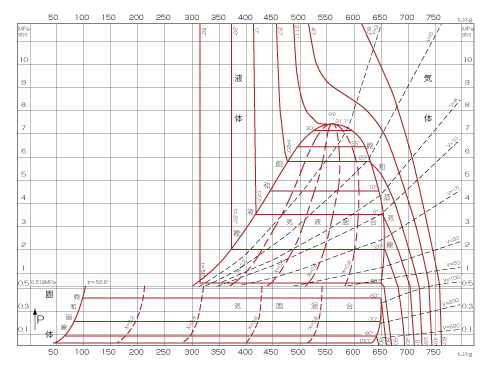
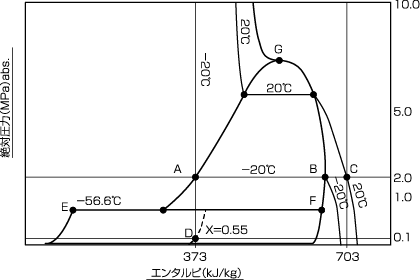
炭酸ガスのエンタルピ線図
- 例−20℃、圧力1.967MPa absの液化炭酸ガス1kgを気化器で熱を与え蒸発させる場合、圧力の変化がなければ、液が全部気化するまで温度の変化はありません。チャート上では、−20℃の等温線(等圧線と重なっている)上をA点からB点に移動し、B点 では完全に気化しています。これを更に20℃まで加熱するとC点に達します。C点のエンタルピは約703kJ、A点のエンタルピが約373kJですから、その差約330kJが1kgの液化炭酸ガス(−20℃)を20℃の気体にするのに必要な熱量になります。 又、A点の液を断熱的にノズルから吹出し大気に放出すると、 等エンタルピ変化をしてD点に達します。この乾き度は0.55ですから、55%が気体に、45%が固体(ドライアイス)になることが分かります。
出典:液化炭酸ガス取扱テキスト 平成18年5月改定